Nessun ormone è stato bistrattato e criminalizzato quanto l’insulina, ritenuta dai sostenitori di diete più o meno pseudoscientifiche la fonte di ogni male: niente di più sbagliato. L’insulina, in realtà, è un ormone chiave per la regolazione di un gran numero di delicati processi fisiologici e solo in particolari condizioni, che nella maggior parte dei casi possono essere evitate con un poco di attenzione, può diventare davvero un problema.
La scoperta dell’insulina
L’11 gennaio del 1922 Leonard Thompson giaceva morente in un letto del Toronto General Hospital, preda di una malattia fino ad allora incurabile: il diabete. Quel giorno, al ragazzo fu iniettata una dose di una sostanza isolata a partire dal pancreas di bovini da Frederick Banting, Charles Best e JJR Macleod, dell’Università di Toronto, con la fondamentale assistenza del biochimico James Collip. Nel giro di poche ore l’elevatissima glicemia del giovane scese a livelli pressoché normali, ma nel sito d’iniezione si sviluppò un brutto ascesso.
Collip tornò immediatamente al lavoro e purificò ulteriormente l’estratto che venne nuovamente iniettato al giovane il 23 gennaio, stavolta senza alcun effetto collaterale e con completo successo: i livelli di glucosio e di chetoni nel sangue del ragazzo tornarono rapidamente normali.
Incoraggiati da questo primo successo, Banting, Best e Collip, trattarono con l’estratto tutti i ricoverati nel reparto che ospitava i soggetti in coma diabetico: prima che arrivassero a iniettare la miracolosa sostanza all’ultimo paziente, i primi giovani che avevano ricevuto il trattamento si stavano già svegliando dal coma, in una scena che sembra tratta di peso da qualche blockbuster hollywoodiano.
Fortunatamente, la scoperta dei quattro ricercatori era reale – un punto di svolta nel trattamento del diabete, una malattia che fino ad allora era a tutti gli effetti una condanna a morte – e valse a Banting e Macleod un premio Nobel, nel 1923, che i due condivisero con Best e Collip, non senza aspre polemiche.
Il nome della sostanza miracolosa, in grado di risvegliare dal coma diabetico quei ragazzi per cui ormai si era persa ogni speranza? Insulina. [1, 2]

Il gruppo di lavoro che per primo ha isolato e utilizzato l’insulina su pazienti diabetici
Cosa è l’insulina?
Il quartetto di Toronto è passato alla storia per aver purificato l’insulina e per averla utilizzata per il trattamento di pazienti diabetici. In realtà, già sul finire dell’800, i tedeschi Minkowski e von Mering avevano ipotizzato che una sostanza prodotta dal pancreas fosse responsabile del controllo dei livelli di glucosio nel sangue, visto che l’asportazione del pancreas in animali da laboratorio provocava il diabete. Seguirono numerosi tentativi di isolare la fantomatica molecola— che il ricercatore belga de Meyer propose di chiamare insulina — tutti infruttuosi, fino al lavoro di Banting e soci.
Nei quasi cento anni che ci separano da quei giorni fatidici che videro la prima applicazione in campo medico sono stati fatti progressi enormi: inizialmente sono state messe a punto tecnologie che hanno permesso di isolare su scala industriale l’insulina animale, per anni l’unica forma disponibile per cura e ricerca. A metà degli anni 60 iniziò la produzione di insulina in laboratorio e nel 1978 si avviò la produzione di insulina umana ricombinante, ottenuta inserendo il gene umano nel genoma di un microrganismo, dapprima un batterio, E. coli, quindi in un lievito, S. Cerevisiae. [3]
Frederick Sanger fu il primo a descrivere in dettaglio la struttura della sostanza, nel 1951, la prima proteina per la quale si riuscì a identificare la completa sequenza degli aminoacidi che la costituiscono.
L’insulina è un ormone peptidico, una proteina prodotta da cellule specializzate del pancreas, le cellule β, localizzate nelle isole di Langerhans, degli agglomerati costituiti da diversi tipi cellulari, ognuno specializzato nella produzione di particolari ormoni.
L’insulina è un dipeptide, è formata cioè da due catene, la catena A costituita da 21 aminoacidi e la catena B che ne conta 30, unite tra loro da due legami che coinvolgono atomi di zolfo presenti in alcuni aminoacidi. Il gene che codifica per l’insulina si trova sul cromosoma 11 e la sua trascrizione porta alla formazione di pre-proinsulina, una struttura complessa formata da un peptide segnale, dalla catena B, dal peptide-C e dalla catena A. La rimozione del peptide segnale porta alla formazione di proinsulina che è accumulata in un particolare organello cellulare, l’apparato di Golgi, un ambiente ricco di calcio e zinco; nel Golgi la proinsulina è convertita per azione di diversi enzimi in insulina matura, formata dalle sole catene A e B, mentre il peptide-C viene rimosso. L’insulina matura a sua volta forma strutture complesse – esameri, contenenti zinco — che vengono secreti in risposta a stimoli specifici. [4, 5]
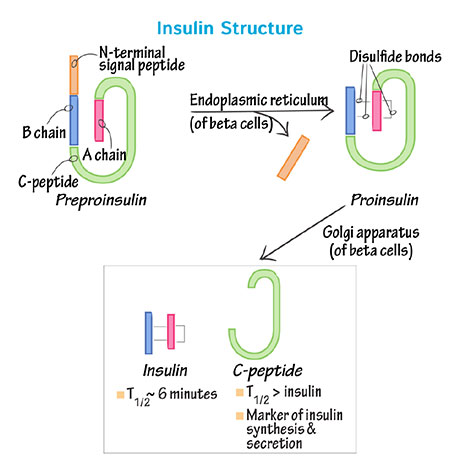
Il processo che porta dalla pre-proinsulina all’insulina matura, in grado di svolgere il suo prezioso ruolo
Qual è la funzione dell’insulina?
Lo stimolo primario per la secrezione dell’ormone è la quantità di glucosio presente in circolo e in effetti il ruolo principale dell’insulina — e del suo ormone antagonista, il glucagone, anch’esso prodotto nel pancreas — è quello di mantenere la glicemia entro un ristretto intervallo di valori. Altri fattori che ne stimolano il rilascio sono concentrazioni elevate di alcuni aminoacidi, in particolar modo arginina, e di acidi grassi liberi.
L’azione dell’enzima è mediata dal suo legame a uno specifico recettore di membrana, l’IRS, di cui esistono quattro varianti, diversamente distribuite nei vari tessuti. Quando l’ormone si lega al suo recettore viene innescata una cascata di reazioni, diversa a livello delle differenti cellule bersaglio. Queste reazioni coinvolgono molteplici vie di segnalazione essenziali nella regolazione del metabolismo — non soltanto dei carboidrati ma anche di lipidi, chetoni e aminoacidi — e di un gran numero di altri processi cellulari, in particolar modo quelli coinvolti nella crescita e nella proliferazione cellulare.
È grazie all’azione dell’insulina che il glucosio in circolo può entrare nelle cellule del tessuto muscolare e di quello adiposo. In condizioni normali il muscolo è responsabile di circa il 60-70% della captazione di glucosio dovuta all’insulina e utilizza il monosaccaride sia per produrre l’energia necessaria alla contrazione muscolare, sia per costituire riserve in forma di glicogeno.
Al tessuto adiposo va appena il 10% del glucosio assorbito grazie all’azione dell’ormone, utilizzato per produrre acidi grassi che in parte sono accumulati negli adipociti, in parte rilasciati in circolo.
L’insulina quindi è un messaggero che comunica alle cellule la disponibilità di materie prime, inibisce l’utilizzo di proteine e glicogeno, promuove il rapido assorbimento di zuccheri, grassi e aminoacidi da parte delle cellule bersaglio e quindi la sintesi di glicogeno e trigliceridi. In pratica, l’insulina è l’ormone dell’abbondanza, il segnale che l’organismo ha tutto quanto serve per crescere. E l’azione dell’insulina nei vertebrati, uomo incluso, si combina con quella dell’ormone della crescita, GH, secreto dall’ipofisi, e quella dell’IGF-1, Insulin-like growth factor 1 — un ormone proteico prodotto nel fegato, con struttura molto simile a quella dell’insulina e in grado di legare gli stessi recettori — per stimolare la sintesi proteica, la crescita, la duplicazione e la proliferazione cellulare. L’IGF-1 è anche un ormone essenziale per lo sviluppo sessuale e per la riproduzione, sia nel maschio che nelle a femmina. L’azione coordinata di questi ormoni determina l’attivazione di una complessa rete di segnalazione cellulare, la via di trasduzione dell’insulina, ISP Insulin-IGFlike signaling pathway, un vero e proprio interruttore in grado di indirizzare la cellula verso crescita e riproduzione o risparmio e longevità.
Quando il cibo è abbondante il livello dell’insulina e degli altri ormoni della famiglia è elevato, l’organismo può crescere, maturare e riprodursi. Quando il cibo è scarso, il livello di insulina e di IGF-1 è ridotto, i recettori rimangono liberi e l’organismo, anziché crescere, impiega la poca energia disponibile per produrre enzimi e proteine che ne aumentano la resistenza allo stress, in attesa di tempi migliori: meccanismo quest’ultimo che è implicato nell’aumento della longevità legato alla restrizione calorica. [6, 7, 8]

Soggetti il cui stile di vita permette all’insulina di svolgere una funzione ottimale
Quando l’insulina diventa un problema
Un dato paradossale viene dagli studi sulla longevità eseguiti sul modello animale, in particolar modo C. elegans, vera e propria superstar della ricerca sul tema: tra questi minuscoli vermi sono i mutanti che non rispondono all’azione dell’insulina e di ormoni simili a presentare una maggiore longevità. In pratica, la resistenza all’insulina aumenta la durata della vita. Proprio il contrario di quanto sappiamo avvenire negli umani, per i quali il progressivo aumento della resistenza all’azione di questo ormone è l’anticamera a tutta una serie di terribili malattie associate all’invecchiamento, dal diabete alle patologie cardiovascolari. Chi presenta insulino-resistenza non vive certo più a lungo anzi, ha un’aspettativa di vita di una decina d’anni inferiore rispetto alla media. Un fatto che potrebbe indurre a ritenere quanto scoperto in organismi modello del tutto ininfluente per la nostra specie. Come sempre, è importante riflettere un attimo, quando i dati raccolti sul modello animale vengono trasferiti all’uomo, non fosse altro che per il notevole livello di complessità che presenta la nostra condizione, dove al dato meramente fisiologico si sovrappongono influenze sociali e culturali.
In una società di cacciatori-raccoglitori la resistenza all’insulina può essere un elemento positivo. Nei periodi in cui la raccolta e la caccia sono particolarmente miseri, la resistenza all’insulina permette comunque di mantenere un adeguato apporto di glucosio agli organi e ai tessuti che ne sono più avidi, in primo luogo il cervello, dirottando le modeste quantità disponibili dagli organi che possono invece utilizzare altri carburanti, principalmente grassi, attivando vie che permettono di resistere allo stress, il tutto a scapito di crescita e riproduzione. Una situazione che conferirebbe un notevole vantaggio adattativo ai soggetti più resistenti all’azione dell’ormone pancreatico.
Un ragionamento di questo tipo è alla base della teoria del “gene risparmiatore”, proposta da Neel[ii] nel 1962, secondo la quale l’elevata incidenza di diabete di tipo II in molte popolazioni – dagli abitanti delle remote isole Nauru, agli indiani Pima del Nuovo Messico – sarebbe dovuta alla selezione di geni che predispongono al diabete, geni che potrebbero essere vantaggiosi per chi vive sotto l’incombente minaccia della fame. L’ipotesi è stata indagata a fondo, non sono stati identificati singoli geni che possano spiegare i fenomeni osservati, e ne sono state proposte un gran numero di possibili varianti.
Indipendentemente dal fatto che esistano o meno i geni risparmiatori, la resistenza all’insulina produce un segnale inequivocabile per il nostro organismo: il cibo è scarso, le risorse sono poche, è il momento di resistere, alla riproduzione penseremo poi.
Il problema nasce nel nostro mondo moderno, dove la disponibilità di cibo è altissima, cibo ricco di zuccheri e grassi, e dove la fame, quella vera, è fortunatamente ignota alla maggior parte di noi, almeno quelli che vivono nel ricco occidente industrializzato. La tipica dieta occidentale determina una concentrazione ematica di glucosio e di altri nutrienti costantemente elevata, che può essere controllata soltanto producendo insulina. Se esiste un certo grado di resistenza all’azione dell’ormone, sarà necessario produrne ancora di più, innescando un circolo vizioso che, soprattutto in individui sedentari, altro grande problema del ricco occidente, porta a un ulteriore aumento della resistenza all’insulina, a una maggior produzione dell’ormone e così via, fino a causare un progressivo esaurirsi della capacità del pancreas che porta alla perdita, più o meno completa, della capacità di controllare la concentrazione di glucosio nel sangue. Seguono diabete, glicazione di proteine, processi ossidativi a carico dei vari tessuti e tutte le altre spiacevoli manifestazioni che abbiamo già visto.
Nella costante abbondanza in cui viviamo la resistenza all’insulina è maladattativa, una conseguenza dell’eccesso e non della privazione, e finisce per causare il diabete e non una maggior longevità, come avviene in C. elegans. Quando il cibo è poco e la glicemia scende inesorabile, l’insulino-resistenza permette all’organismo di sopportare le durezze dell’ambiente, grazie ad adattamenti che permettono di sopravvivere fino al termine della carestia. Quando si vive nell’abbondanza perenne l’insulino-resistenza diventa invece un elemento assolutamente negativo, uno dei fattori che contribuiscono ai processi d’invecchiamento.
L’insulina è un segnale, la cui secrezione è determinata a sua volta dall’integrazione di altri segnali che provengono da una intricata rete di sensori, in risposta a variazioni dell’ambiente esterno e interno. È probabile che ci siano dei livelli ottimali per l’azione dell’insulina, diversi tra le specie, ma cruciali nella regolazione non soltanto di processi metabolici ma anche dello sviluppo e della longevità. L’insulina non è buona o cattiva, queste sono categorie che noi assegniamo in maniera arbitraria a processi fisiologici che hanno come obiettivo quello di permettere al sistema di funzionare al meglio, qualunque cosa avvenga. L’insulina può diventare un problema quando il nostro stile di vita è sbagliato, quando noi stessi contribuiamo a creare le condizioni che sono alla radice del problema. Abbiamo dalla nostra due strumenti potenti per far sì che il segnale lavori per noi; una dieta misurata, che permette di evitare una secrezione eccessiva dell’ormone, e l’attività fisica, che permette di mantenere elevata la sensibilità al segnale da parte del tessuto muscolare, di solito, nel sedentario, la prima vittima dell’insulino-resistenza, con un effetto domino dalle conseguenze nefaste. [9, 10, 11, 12]